
通常情况下,将二氧化碳气体直接通入装有氢氧化钠溶液的试管中,由于没有明显的外观现象很难直接判断二氧化碳气体与氢氧化钠溶液是否反应。因此,要判断二氧化碳气体确实能与氢氧化钠溶液反应,可以采取如下两种方法:
(1)检验产物:验证通入二氧化碳气体后的溶液中是否含有碳酸钠,检验碳酸根离子是否存在。通常检验碳酸根离子的方法是:
方法1:取样,加入稀盐酸,并将产生的气体通入澄清石灰水中,若澄清石灰水变浑浊,则证明溶液中存在碳酸根离子。
方法2:取样,加入澄清石灰水,若产生白色沉淀,则证明溶液中存在碳酸根离子。
上述两种方法也可以检验氢氧化钠溶液是否变质。

(2)改进实验装置,通过一些明显的实验现象间接证明二氧化碳气体能与氢氧化钠反应(利用CO2气体与氢氧化钠溶液反应后气体减少,压强变小的原理)。如:
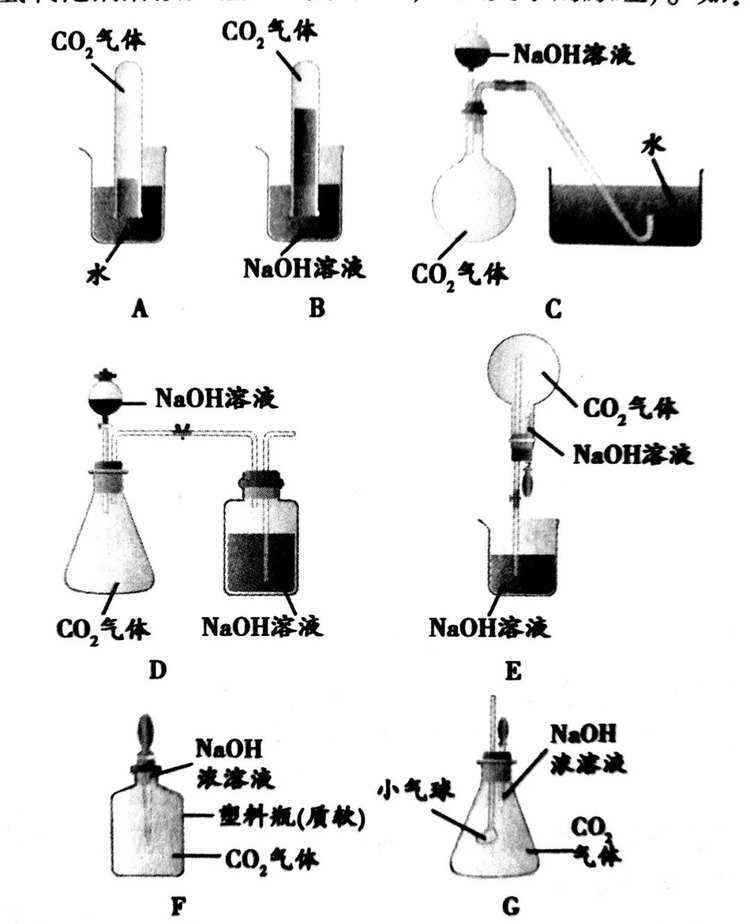

通过观察形变的方法来验证氢氧化钠溶液与二氧提化碳的反应,需要排除二氧化碳溶于水产生的质疑,这样才能使实验更具有科学性。

例2在学习碱的性质时,为了验证溶液中的氢氧化钠能与二氧化碳反应,老师做了下面两个实验。

实验一:如图甲,将一支充满二氧化碳的试管倒扣在盛有氢氧化钠溶液的烧杯中,观察试管中的液面变化情况。
实验二:如图乙,向两个装满二氧化碳的同样规格的集气瓶中分别注入等量的氢氧化钠溶液和蒸馏水,观察U形管(装有红墨水)两端液面的变化情况。
(1)实验二中若观察到U形管左端液面 (填“升高”或“降低”),则证明溶液中的氢氧化钠能与二氧化碳反应。
(2)与实验一相比,同学们认为实验二更合理,因为实验二能排除 对实验的干扰。

(解析)(1)CO2与NaOH反应,反应消耗了气体,左侧集气瓶中压强减小;CO2能溶于水且能与水反应,故右侧集气瓶内压强也减小,但气压减小程度比左侧小,从而导致U形管左端液面升高。
(2)实验一中试管内液面上升,虽有明显现象,但不能排除水的干扰(二氧化碳能溶于水,也可与水反应);实验二中通过U形管中出现了液面差,说明二氧化碳与氢氧化钠发生了反应。
答案(1)升高(2)水

本文由初中化学大师原创,欢迎关注,一起涨知识!
允许非盈利性引用,并请注明出处:“转载自初中化学大师”字样,以尊重作者的劳动成果。版权归原作/译者所有。未经允许,对非法转载者,保留采用法律手段追究的权利。